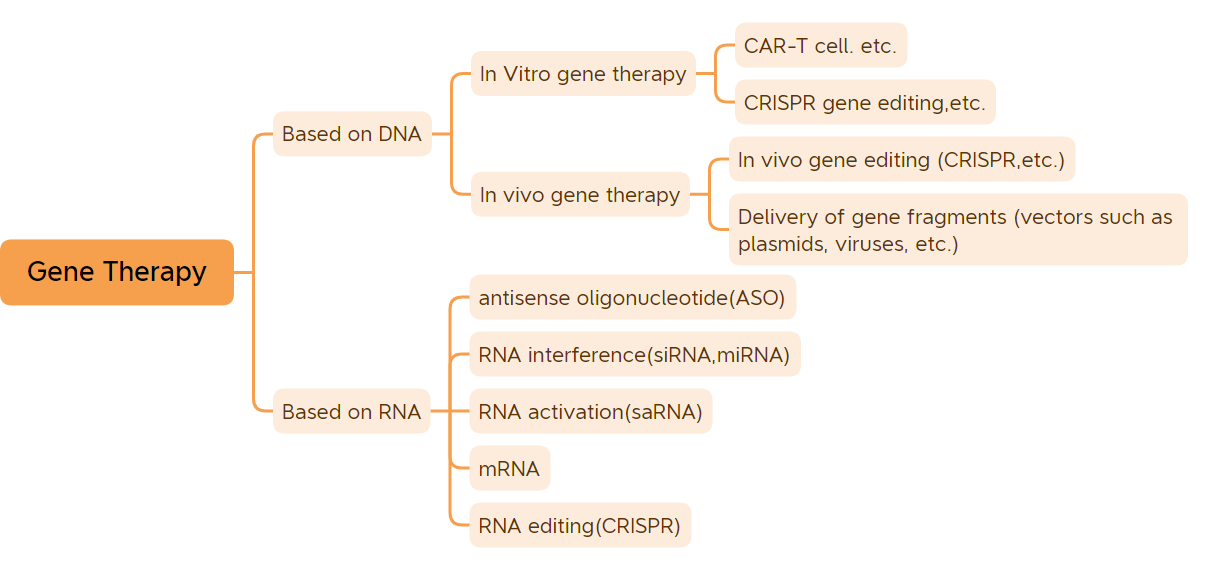
Гендер - белгилерди башкаруучу негизги генетикалык бирдиктер.Кээ бир вирустардын РНКдан турган гендеринен башкасы, көпчүлүк организмдердин гендери ДНКдан турат..Организмдердин ооруларынын көбү гендер менен айлана-чөйрөнүн өз ара аракетинен келип чыгат.Ген терапиясы негизинен көптөгөн ооруларды айыктыра алат.Ген терапиясы медицина жана фармацевтика тармагындагы революция болуп эсептелет.Кеңири мааниде ген терапиясы препараттарына ДНК-модификацияланган ДНК препараттарына негизделген (мисалы, вирустук векторлордун негизиндеги in vivo ген терапиясы препараттары, in vitro ген терапиясы препараттары, жылаңач плазмиддик дарылар ж.б.) жана РНК препараттары (мисалы, антисенстик олигонуклеотиддик дарылар, siRNA препараттары жана мРНК терапиясы ж.б.) кирет.тар маанидеги ген терапиясы препараттарына негизинен плазмиддик ДНК препараттары, вирустук векторлорго негизделген ген терапиясы препараттары, бактериялык векторлорго негизделген ген терапиясы препараттары, генди редакциялоо системалары жана in vitro генди модификациялоо үчүн клетка терапиясы препараттары кирет.Көп жылдар бою кыйшаюусуз өнүгүүдөн кийин ген терапиясынын дарылары бекемдээрлик клиникалык натыйжаларга жетишти.(ДНК вакциналарын жана мРНК вакциналарын эсепке албаганда) Учурда дүйнөдө 45 ген терапиясы дары маркетинг үчүн бекитилген.Быйыл маркетинг үчүн жалпысынан 9 ген терапиясы бекитилген, анын ичинде быйыл биринчи жолу маркетинг үчүн бекитилген 7 ген терапиясы, атап айтканда: CARVYKTI, Amvuttra, Upstaza, Roctavian, Hemgenix, Adstiladrin жана Ebvallo, (Эскертүү: Калган экөө ушул жылы Кошмо Штаттарда бекитилген. 2022-жылдын августунда Америка Кошмо Штаттарында маркетинг үчүн DA жана 2019-жылы Европа Биримдиги тарабынан маркетинг үчүн бекитилген; .) Барган сайын көбүрөөк ген терапиясынын продуктуларынын ишке кириши жана ген терапиясынын технологиясынын тез өнүгүшү менен ген терапиясы тез өнүгүү мезгилин баштамакчы.
Ген терапиясынын классификациясы (Сүрөт булагы: Bio-Matrix)
Бул макалада маркетинг үчүн бекитилген 45 ген терапиясы (ДНК вакциналарынан жана mRNA вакциналарынан тышкары) тизмеленген.
1. In vitro ген терапиясы
(1) Strimvelis
Компания: GlaxoSmithKline (GSK) тарабынан иштелип чыккан.
Базарга чыгуу убактысы: 2016-жылдын май айында Европа Биримдиги тарабынан маркетинг үчүн бекитилген.
Көрсөтмөлөрү: Оор айкалышкан иммундук жетишсиздикти (SCID) дарылоо үчүн.
Эскертүү: Бул терапиянын жалпы процесси адегенде пациенттин өзүнүн гемопоэтикалык өзөк клеткаларын алуу, аларды in vitro кеңейтүү жана өстүрүү, андан кийин гемопоэтикалык өзөк клеткаларына функционалдык ADA (аденозиндеаминаза) генинин көчүрмөсүн киргизүү үчүн ретровирусту колдонуу жана акырында модификацияланган гемопоэтикалык өзөк клеткаларын инъекциялоо болуп саналат.Клиникалык натыйжалар Strimvelis менен дарыланган ADA-SCID бейтаптардын 3 жылдык жашоо көрсөткүчү 100% экенин көрсөтүп турат.
(2) Залмоксис
Компания: Италиянын MolMed компаниясы тарабынан чыгарылган.
Базарга чыгуу убактысы: 2016-жылы Европа Биримдигинен шарттуу маркетинг уруксатын алган.
Көрсөтмөлөрү: Гемопоэтикалык өзөк клеткасын трансплантациялоодон кийин пациенттердин иммундук системасынын адъюванттык терапиясы үчүн колдонулат.
Эскертүү: Залмоксис – бул ретровирустук векторлор тарабынан өзгөртүлгөн аллогендик Т-клеткалык суицид генинин иммунотерапиясы.Бул метод аллогендик Т-клеткаларды генетикалык жактан модификациялоо үчүн ретровирустук векторлорду колдонот, ошону менен генетикалык жактан өзгөртүлгөн Т-клеткалар 1NGFR жана HSV-TK Mut2 суицид гендерин экспрессиялайт, адамдарга терс иммундук реакцияларды пайда кылган Т-клеткаларды өлтүрүү үчүн каалаган убакта ганцикловир (ганцикловир) препараттарын колдонууга мүмкүндүк берет, иммундук системанын бузулушуна жол бербөө жана GVHD пациенттеринин иммундук реконструкциядан кийинки функцияларынын реконструкциясын камсыз кылат. скорт.
(3) Invossa-K
Компания: TissueGene (KolonTissueGene) тарабынан иштелип чыккан.
Базарга чыгуу убактысы: 2017-жылдын июлунда Түштүк Кореяда листингге бекитилген.
Көрсөтмөлөр: дегенеративдик тизе артритин дарылоо үчүн.
Эскертүү: Invossa-K адамдын хондроциттерин камтыган аллогендик клетка ген терапиясы.Аллогендик клеткалар in vitro генетикалык жактан өзгөртүлгөн жана өзгөртүлгөн клеткалар артикулярдык инъекциядан кийин трансформациялоочу өсүү факторун β1 (TGF-β1) экспрессиялап, бөлүп чыгара алышат.β1), ошону менен остеоартриттин белгилерин жакшыртат.Клиникалык натыйжалар Invossa-K олуттуу тизе артрит жакшыртууга мүмкүн экенин көрсөтүп турат.Ал 2019-жылы Кореянын Азык-түлүк жана дары-дармек башкармалыгы тарабынан жокко чыгарылган, анткени өндүрүүчү колдонулган ингредиенттерди туура эмес белгилеп койгон.
(4) Zynteglo
Компания: Bluebird bio тарабынан изилденген жана иштелип чыккан.
Базарга чыгуу убактысы: 2019-жылы маркетинг үчүн Европа Биримдиги тарабынан жактырылган жана 2022-жылдын августунда АКШда маркетинг үчүн FDA тарабынан бекитилген.
Көрсөтмөлөр: Трансфузияга көз каранды β-талассемияны дарылоо үчүн.
Эскертүү: Зинтегло – бул лентивируалдык in vitro ген терапиясы, ал бейтаптан lentiviral вектор аркылуу алынган гемопоэтикалык өзөк клеткаларына нормалдуу β-глобин генинин (βA-T87Q-глобин гени) функционалдык көчүрмөсүн киргизет, андан кийин бул генетикалык жактан модификацияланган аутологдук гематопо клеткаларына кайра инфузиялайт.Оорулуу нормалдуу βA-T87Q-глобин генине ээ болгондон кийин, алар кан куюуга болгон муктаждыкты натыйжалуу азайта же жок кыла турган кадимки HbAT87Q протеинди өндүрө алышат.Бул 12 жаштагы жана андан улуу бейтаптар үчүн өмүр бою кан куюу жана өмүр бою дарыларды алмаштыруу үчүн арналган бир жолку терапия.
(5) Skysona
Компания: Bluebird bio тарабынан изилденген жана иштелип чыккан.
Базарга чыгуу убактысы: 2021-жылдын июлунда маркетинг үчүн Европа Биримдиги тарабынан жактырылган жана 2022-жылдын сентябрында АКШда маркетинг үчүн FDA тарабынан бекитилген.
Көрсөтмөлөр: эрте мээнин адренолейкодистрофиясын (CALD) дарылоо үчүн.
Эскертүү: Skysona ген терапиясы мээнин адренолевкодистрофиясынын башталышын (CALD) дарылоо үчүн бекитилген жалгыз бир жолку ген терапиясы.Skysona (elivaldogene autotemcel, Lenti-D) гемопоэтикалык өзөк клеткасы lentiviral in vitro ген терапиясы Lenti-D болуп саналат.Терапиянын жалпы жол-жобосу төмөнкүдөй: аутологиялык гемопоэтикалык өзөк клеткалары пациенттен алынып, трансдукцияланып, адамдын ABCD1 генин алып жүрүүчү лентивирус аркылуу in vitro аркылуу модификацияланат, андан кийин пациентке кайра куюлат.Бул ABCD1 ген мутациясын алып жүрүүчү 18 жашка чейинки бейтаптарды жана CALD дарылоо үчүн колдонулат.
(6) Кымрия
КОМПАНИЯ: Novartis тарабынан иштелип чыккан.
Базарга чыгуу убактысы: 2017-жылдын августунда маркетинг үчүн FDA тарабынан бекитилген.
Көрсөтмөлөр: прекурсордук В-клеткалык курч лимфобластикалык лейкозду (ALL) жана рецидивдүү жана отко чыдамдуу DLBCLди дарылоо.
Эскертүү: Kymriah - бул лентивирустук in vitro ген терапиясы дары, дүйнөдө маркетинг үчүн бекитилген биринчи CAR-T терапиясы, CD19га багытталган жана 4-1BB ко-стимулдаштыруучу факторду колдонгон.Анын баасы АКШда 475 000 доллар, Японияда 313 000 доллар.
(7) Yescarta
Компания: Gilead (GILD) туунду компаниясы Kite Pharma тарабынан иштелип чыккан.
Базарга чыгуу убактысы: 2017-жылдын октябрында маркетинг үчүн FDA тарабынан бекитилген;Fosun Kite Kite Pharma компаниясынан Yescarta технологиясын киргизип, уруксат алгандан кийин Кытайда чыгарган.Өлкөдө листингге бекитилген.
Көрсөтмөлөр: рецидивдүү же отко чыдамдуу чоң В-клеткалуу лимфоманы дарылоо үчүн.
Эскертүү: Yescarta – бул ретровирустук in vitro ген терапиясы, бул дүйнөдө экинчи бекитилген CAR-T терапиясы.Ал CD19га багытталган жана CD28дин костимуляторун кабыл алат.Анын АКШда баасы 373 миң доллар.
(8) Tecartus
Компания: Гилат тарабынан иштелип чыккан (GILD).
Базарга чыгуу убактысы: FDA тарабынан 2020-жылдын июлунда маркетинг үчүн бекитилген.
Көрсөтмөлөр: рецидивдүү же отко чыдамдуу мантия клеткасынын лимфомасы үчүн.
Эскертүү: Tecartus CD19га багытталган аутологиялык CAR-T клетка терапиясы жана бул дүйнөдө маркетинг үчүн бекитилген үчүнчү CAR-T терапиясы.
(9) Breyanzi
КОМПАНИЯ: Bristol-Myers Squibb (BMS) тарабынан иштелип чыккан.
Базарга чыгуу убактысы: FDA тарабынан 2021-жылдын февралында маркетинг үчүн бекитилген.
Көрсөтмөлөр: Рецидивдүү же рефракциялык (R/R) чоң В-клеткалык лимфома (LBCL).
Эскертүү: Breyanzi бул лентивируска негизделген in vitro ген терапиясы, CD19га багытталган дүйнөдө маркетинг үчүн бекитилген төртүнчү CAR-T терапиясы.Бреянзинин жактырылышы Бристол-Майерс Сквибб үчүн уюлдук иммунотерапия тармагындагы маанилүү этап болуп саналат, ал 2019-жылы Celgeneди 74 миллиард долларга сатып алганда алган.
(10) Абекма
Компания: Bristol-Myers Squibb (BMS) жана bluebird bio тарабынан биргелешип иштелип чыккан.
Базарга чыгуу убактысы: FDA тарабынан 2021-жылдын март айында маркетинг үчүн бекитилген.
Көрсөтмөлөр: рецидивдүү же рефрактериялык көп миелома.
Эскертүү: Abecma бул лентивируска негизделген in vitro ген терапиясы, BCMAга багытталган дүйнөдөгү биринчи CAR-T клетка терапиясы жана FDA тарабынан бекитилген бешинчи CAR-T терапиясы.Дарынын принциби лентивирус аркылуу генди in vitro модификациялоо аркылуу пациенттин Т-клеткаларында химерикалык BCMA рецепторлорун экспрессиялоо болуп саналат.Дарылоо бейтаптарда генетикалык жактан өзгөртүлбөгөн Т-клеткаларды жок кылуу, андан кийин бейтаптарда BCMA-экспрессиялоочу рак клеткаларын издеп жана өлтүргөн өзгөртүлгөн Т-клеткаларды кайра куюу.
(11) Libmeldy
КОМПАНИЯ: Orchard Therapeutics тарабынан иштелип чыккан.
Базарга чыгуу убактысы: 2020-жылдын декабрында листингге Европа Биримдиги тарабынан бекитилген.
Көрсөтмөлөр: метахроматикалык лейкодистрофияны (МЛД) дарылоо үчүн.
Эскертүү: Libmeldy - лентивирус менен in vitro генетикалык жактан өзгөртүлгөн аутологиялык CD34+ клеткаларына негизделген ген терапиясы.Клиникалык маалыматтар көрсөткөндөй, Либмелдинин бир жолу венага инфузиясы ошол эле курактагы дарыланбаган бейтаптардагы мотор жана когнитивдик бузулууларга салыштырмалуу эрте башталган MLDнин жүрүшүн эффективдүү өзгөртө алат.
(12) Бенода
Компания: WuXi Giant Nuo тарабынан иштелип чыккан.
Базарга чыгуу убактысы: NMPA тарабынан 2021-жылдын сентябрында расмий түрдө бекитилген.
Көрсөтмөлөр: экинчи линиядагы же андан жогору системалуу терапиядан кийин кайра кайталанган же рефрактикалык чоң В-клеткалык лимфомасы (r/r LBCL) менен ооруган чоң кишилерди дарылоо.
Эскертүү: Бейнода анти-CD19 CAR-T ген терапиясы болуп саналат, ошондой эле WuXi Juro компаниясынын негизги продуктусу.Бул Кытайда жактырылган экинчи CAR-T продуктусу, рецидивдүү / отко чыдамдуу чоң В-клеткалык лимфоидден башка ВуХи Гигант Нуо дагы бир нече башка көрсөткүчтөрдү, анын ичинде фолликулярдык лимфоманы (FL), мантия клеткасынын лимфомасын (MCL), өнөкөт лимфоциталдык лимфоцитти (ЛЛЛ-ЛЛ-КЛ) дарылоо үчүн Regiorensai инъекциясын иштеп чыгууну пландаштырууда. ma (DLBCL) жана курч лимфобластикалык лейкоз (ALL).
(13) CARVYKTI
Компания: Legend Biotech компаниясынын биринчи продуктусу маркетинг үчүн бекитилген.
Базарга чыгуу убактысы: FDA тарабынан 2022-жылдын февралында маркетинг үчүн бекитилген.
Көрсөтмөлөр: рецидивдүү же рефрактикалык көп миеломаны (R/R MM) дарылоо үчүн.
Эскертүү: CARVYKTI (ciltacabtagene autoleucel, кыскача Cilta-cel) - бул CAR-T клеткасынын иммундук ген терапиясы, В-клеткасынын жетилген антигенине (BCMA) багытталган эки домендүү антителолор.Маалыматтар көрсөткөндөй, CARVYKTI Рецидивдүү же рефрактериялык көп миелома менен ооруган бейтаптарда төрт же андан көп мурда терапия алган (анын ичинде протеазома ингибиторлору, иммуномодуляторлор жана анти-CD38 моноклоналдык антителолору) жалпы жооптун деңгээли 98%ды түзгөн.
(14)Эбвалло
КОМПАНИЯ: Atara Biotherapeutics тарабынан иштелип чыккан.
2022-жылдын декабрында маркетинг боюнча Европа Комиссиясы (EC) маркетинг үчүн бекитилген дүйнөдөгү биринчи универсалдуу Т клетка терапиясы.
Көрсөтмөлөр: Эпштейн-Барр вирусу (EBV) менен байланышкан трансплантациядан кийинки лимфопролиферативдик оорунун (EBV+PTLD) монотерапиясы катары дарыланып жаткан бейтаптар чоңдор жана 2 жаштан жогорку балдар болушу керек, алар мурда жок дегенде бир башка дары-дармек терапиясын алган.
Эскертүү: Эбвалло - бул аллогендик EBV-спецификалык универсалдуу Т-клетка ген терапиясы, ал HLA-чектелген ыкмада EBV жуккан клеткаларды бутага алат жана жок кылат.Бул терапияны бекитүү негизги фазадагы 3 клиникалык изилдөөнүн жыйынтыгына негизделген жана натыйжалар HCT тобунун жана SOT тобунун ORR 50% түзөөрүн көрсөттү.Толук ремиссия (CR) көрсөткүчү 26,3%, жарым-жартылай ремиссия (PR) 23,7% жана ремиссияга чейинки орточо убакыт (ТР) 1,1 айды түздү.Ремиссияга жетишкен 19 бейтаптын 11инде 6 айдан ашык жооп узактыгы (DOR) болгон.Мындан тышкары, коопсуздук жагынан алганда, трансплант-каршы-хост оорусу (GvHD) же Эбвалло менен байланышкан цитокиндерди чыгаруу синдрому сыяктуу терс реакциялар болгон эмес.
2. Вирустук векторлорго негизделген in vivo ген терапиясы
(1) Gendicine/Jin Sheng
Компания: Shenzhen Saibainuo компаниясы тарабынан иштелип чыккан.
Базарга чыгуу убактысы: 2003-жылы Кытайда листингге бекитилген.
Көрсөтмөлөр: баш жана моюндун сквамуоздук рак оорусун дарылоо үчүн.
Эскертүү: Рекомбинантты адам p53 аденовирус инъекциясы Gendicine/Jinyousheng - бул Shenzhen Saibainuo компаниясына таандык көз карандысыз интеллектуалдык менчик укугу бар аденовирус вектордук ген терапиясы.Адамдын 5-типтеги аденовирусу адамдын 5-типтеги аденовирусунан турат. Биринчиси дарынын шишикке каршы эффектисинин негизги структурасы болуп саналат, ал эми экинчиси негизинен алып жүрүүчү катары иштейт.Аденовирус вектору p53 терапиялык генин максаттуу клеткага алып барат, максаттуу клеткада p53 шишик басуучу генин экспрессиялайт жана анын ген экспрессиясы Продукт ар кандай ракка каршы гендерди жогорулатып, ар кандай онкогендердин иш-аракеттерин төмөндөтүп, ошону менен организмдин шишиктерди басуучу жана өлтүрүүчү таасирин күчөтөт.
(2) Ригвир
Компания: Латима компаниясы тарабынан иштелип чыккан, Латвия.
Листинг убактысы: 2004-жылы Латвияда листингге бекитилген.
Көрсөтмөлөрү: Меланоманы дарылоо үчүн.
Эскертүү: Ригвир – генетикалык жактан өзгөртүлгөн ECHO-7 энтеровирус векторунун негизиндеги ген терапиясы.Учурда дары Латвияда, Эстонияда, Польшада, Арменияда, Белоруссияда ж.б. кабыл алынган, ошондой эле ЕБ өлкөлөрүндө EMA каттоодон өтүп жатат.Акыркы он жылдагы клиникалык учурлар Ригвир онколитикалык вирусунун коопсуз жана эффективдүү экендигин далилдеп, меланома менен ооругандардын жашоо деңгээлин 4-6 эсеге көбөйтөт.Мындан тышкары, бул терапия башка рак ооруларына да колдонулат, анын ичинде ичеги рагы, уйку безинин рагы, табарсык рагы, бөйрөк рагы, простата рагы, өпкө рагы, жатын рагы, лимфосаркома ж.б.
(3) Онкорин
Компания: Shanghai Sanwei Biological Company тарабынан иштелип чыккан.
Базарга чыгуу убактысы: 2005-жылы Кытайда листингге бекитилген.
Көрсөтмөлөрү: баш жана моюн шишиктерин, боор рагын, уйку безинин рагын, жатын моюнчасынын рагын жана башка рактарды дарылоо.
Эскертүү: Oncorine (安科瑞) – аденовирусту алып жүрүүчү катары колдонгон онколитикалык вирус ген терапиясы.Онколитикалык аденовирус алынат, ал p53 гени жетишсиз же анормалдуу шишиктерде өзгөчө көбөйүп, шишик клеткаларынын лизисине алып келип, шишик клеткаларын өлтүрөт.нормалдуу клеткаларга зыян келтирбестен.Клиникалык изилдөөлөр Ankerui зыяндуу шишиктердин ар кандай жакшы коопсуздук жана натыйжалуулугун көрсөттү.
(4) Глибера
Компания: uniQure тарабынан иштелип чыккан.
Базарга чыгуу убактысы: 2012-жылы Европада листингге бекитилген.
Көрсөтмөлөр: катуу чектелген майлуу диетага карабастан, панкреатиттин катуу же кайталануучу эпизоддору менен липопротеин-липаза жетишсиздигин (LPLD) дарылоо.
Эскертүү: Glybera (alipogene tiparvovec) AAV негизинде ген терапиясы дары болуп саналат, ал AAV терапиялык ген LPL булчуң клеткаларына трансдукциялоочу катары колдонот, ошондуктан тиешелүү клеткалар белгилүү бир өлчөмдө липопротеин липазасын чыгара алат.Дары рыноктон 2017-жылы чыгарылган. Анын алынышынын себеби эки факторго байланыштуу болушу мүмкүн: жогорку баа жана рыноктун чектелген талабы.Дарыны дарылоонун орточо баасы 1 миллион АКШ долларын түзөт жана азырынча бир гана бейтап аны сатып алып, колдонгон.Медициналык камсыздандыруу компаниясы ал үчүн 900 000 АКШ долларын кайтарып бергенине карабастан, бул камсыздандыруу компаниясы үчүн салыштырмалуу чоң жүк.Мындан тышкары, дары багытталган көрсөткүчтөр өтө сейрек кездешет, оорунун көрсөткүчү 1 миллионго жакын жана туура эмес диагноз коюунун жогорку көрсөткүчү.
(5) Imlygic
Компания: Amgen тарабынан иштелип чыккан.
Базарга чыгуу убактысы: 2015-жылы ал Америка Кошмо Штаттарынын жана Европа Бирлигинин тизмесине бекитилди.
Көрсөтмөлөр: хирургиялык жол менен толугу менен жок кылынбаган меланома жараларын дарылоо.
Эскертүү: Imlygic – бул генетикалык технология менен модификацияланган (анын ICP34.5 жана ICP47 ген фрагменттерин жок кылуу жана вируска адамдын гранулоцитинин макрофагынын колониясын стимулдаштыруучу фактор GM-CSF генин киргизүү) тарабынан өзгөртүлгөн 1 типтеги жөнөкөй герпес вирусу.Башкаруу ыкмасы шишик клеткаларынын жарылып кетишине, шишиктен алынган антигендерди жана GM-CSFди чыгарууга жана шишикке каршы иммундук реакцияларды жайылтуу үчүн меланома жараларына түздөн-түз сайылышы мүмкүн болгон интралезиялык инъекция болуп саналат.
(6) Люкстурна
Компания: Spark Therapeutics тарабынан иштелип чыккан, Roche туунду компаниясы.
Базарга чыгуу убактысы: 2017-жылы FDA тарабынан маркетинг үчүн бекитилген, андан кийин 2018-жылы Европада маркетинг үчүн бекитилген.
Көрсөтмөлөр: кош копиялуу RPE65 ген мутацияларынан улам көрүүсүн жоготкон, бирок жетиштүү сандагы жашоого жөндөмдүү торчо клеткаларын сактап калган балдарды жана чоң кишилерди дарылоо үчүн.
Эскертүү: Luxturna subretinal сайынуу тарабынан башкарылуучу AAV негизделген ген терапиясы болуп саналат.Ген терапиясы AAV2ди алып жүрүүчү катары кадимки RPE65 генинин функционалдык көчүрмөсүн пациенттин торчосу клеткаларына киргизүү үчүн колдонот, ошондуктан тиешелүү клеткалар кадимки RPE65 протеинди экспрессиялап, пациенттин RPE65 белоктун жетишсиздигин толуктап, ошону менен пациенттин көрүүсүн жакшыртат.
(7) Zolgensma
Компания: AveXis тарабынан иштелип чыккан, Novartis туунду компаниясы.
Базарга чыгуу убактысы: FDA тарабынан 2019-жылдын май айында маркетинг үчүн бекитилген.
Көрсөтмөлөр: Омуртка булчуңдарынын атрофиясы (SMA) 2 жашка чейинки бейтаптарды дарылоо.
Эскертүү: Zolgensma - AAV векторунун негизиндеги ген терапиясы.Бул дары дүйнөдө маркетинг үчүн бекитилген жүлүн булчуң атрофиясы үчүн бир жолку дарылоо планы болуп саналат.Дарыны ишке киргизүү омуртка булчуңдарынын атрофиясын дарылоодо жаңы доорду ачат.бет, маанилүү кадам болуп саналат.Бул ген терапиясы scAAV9 векторун пациентке кадимки SMN1 генин тамырга инфузия аркылуу киргизүү үчүн колдонот, бул нормалдуу SMN1 протеинди өндүрүү, ошону менен мотор нейрондору сыяктуу жабыркаган клеткалардын функциясын жакшыртат.Ал эми, SMA дары Spinraza жана Evrysdi узак мөөнөттүү кайталап дозасын талап кылат.Spinraza ар бир төрт ай омуртка сайынуу менен берилет, жана Evrysdi күнүмдүк оозеки дары болуп саналат.
(8) Delytact
Компания: Daiichi Sankyo Company Limited тарабынан иштелип чыккан (TYO: 4568).
Базарга чыгуу убактысы: 2021-жылдын июнь айында Япониянын Саламаттыкты сактоо, эмгек жана бакубатчылык министрлигинен (MHLW) шарттуу макулдук.
Көрсөтмөлөрү: Зыяндуу глиоманы дарылоо үчүн.
Эскертүү: Delytact - бул төртүнчү онколиттик вирустун ген терапиясы, ошондой эле залалдуу глиоманы дарылоо үчүн бекитилген биринчи онколитикалык вирус продуктусу.Delytact бул гендик инженерияланган жөнөкөй герпес вирусунун 1 түрү (HSV-1) онколитикалык вирусу, доктор Тодо жана кесиптештери тарабынан иштелип чыккан.Delytact экинчи муундагы HSV-1 G207 геномуна кошумча жок кылуу мутацияларын киргизип, анын рак клеткаларында тандалма репликациясын жана жогорку коопсуздукту сактоо менен шишикке каршы иммундук жоопторду индукциялоону күчөтөт.Delytact учурда клиникалык баалоодон өтүп жаткан биринчи үчүнчү муундагы онколитикалык HSV-1.Японияда Delytact бекитүү, негизинен, бир колу-фаза 2 клиникалык сыноого негизделген.Кайталануучу глиобластома менен ооруган бейтаптарда Delytact бир жылдык жашоо көрсөткүчүнүн негизги акыркы чекитине жетишти жана натыйжалар Delytact G207ге салыштырмалуу жакшыраак натыйжалуулугун көрсөттү.Күчтүү репликативдик күч жана жогорку шишикке каршы активдүүлүк.Бул эмчек, простата, schwannomas, мурун-тамак, гепатоцеллюлярдык, колоректалдык, зыяндуу перифериялык нерв кабыгынын шишиктери жана калкан безинин рактын катуу шишик моделдеринде натыйжалуу болгон.
(9) Upstaza
КОМПАНИЯ: PTC Therapeutics, Inc. тарабынан иштелип чыккан (NASDAQ: PTCT).
Базарга чыгуу убактысы: 2022-жылдын июлунда маркетинг үчүн Европа Биримдиги тарабынан бекитилген.
Көрсөтмөлөр: Ароматтык L-аминокислота декарбоксилазасынын (AADC) жетишсиздиги үчүн 18 ай жана андан улуу бейтаптарды дарылоо үчүн бекитилген.
Эскертүү: Upstaza™ (eladocagene exuparvovec) – алып жүрүүчү катары адено-ассоциацияланган 2 типтеги вирус (AAV2) менен in vivo ген терапиясы.Бейтаптар AADC ферментин коддоочу гендеги мутациялардан улам ооруп калышат.AAV2 AADC энзимин коддоочу дени сак генди алып жүрөт.ген компенсация формасы терапиялык эффектке жетет.Теориялык жактан алганда, бир башкаруу узак убакыт бою натыйжалуу болот.Бул түздөн-түз мээге сайылган биринчи сатылган ген терапиясы.Маркетингдик уруксат ЕСтин бардык 27 мүчө-мамлекеттерине, ошондой эле Исландия, Норвегия жана Лихтенштейнге тиешелүү.
(10) Roctavian
Компания: BioMarin Pharmaceutical (BioMarin) тарабынан иштелип чыккан.
Базарга чыгуу убактысы: 2022-жылдын августунда Европа Биримдиги тарабынан маркетинг үчүн бекитилген;Улуу Британиянын Дары-дармек жана саламаттыкты сактоо продуктылары башкармалыгы (MHRA) тарабынан 2022-жылдын ноябрында маркетинг уруксаты.
Көрсөтмөлөр: FVIII факторунун ингибирлөө тарыхы жок жана AAV5 антителолоруна терс таасирин тийгизген оор гемофилия А менен ооруган чоң кишилерди дарылоо үчүн.
Эскертүү: Roctavian (valoctocogene roxaparvovec) AAV5ти вектор катары колдонот жана В домени жок кылынган адамдын коагуляция факторунун VIII (FVIII) экспрессиясын жүргүзүү үчүн адамдын бооруна тиешелүү HLP промоутарын колдонот.Еврокомиссиянын valoctocogene roxaparvovec маркетингин бекитүү чечими дары-дармектин клиникалык өнүгүү долбоорунун жалпы маалыматтарына негизделген.Алардын ичинен III фазадагы GENER8-1 клиникалык сыноосунун жыйынтыгы көрсөткөндөй, кабыл алынганга чейинки жылдын маалыматтары менен салыштырганда, валоктокоген роксапарвовектин бир жолу инфузиясынан кийин сыналуучунун жылдык кан кетүү ылдамдыгы (АБР) кыйла азайган, рекомбинанттык коагуляция факторун колдонуу жыштыгы VIII (F8) же кандагы протеиндин активдүүлүгү кескин төмөндөгөн.4 жумалык дарылоодон кийин, субъекттин жылдык F8 колдонуу курсу жана дарылоону талап кылган ABR тиешелүүлүгүнө жараша 99% жана 84% га кыскарган жана айырма статистикалык жактан маанилүү болгон (p<0.001).Коопсуздук профили жакшы болгон жана эч бир субъект F8 факторунун ингибициясын, залалдуу же тромбоздун терс таасирлерин байкаган эмес жана дарылоого байланыштуу олуттуу жагымсыз окуялар (SAEs) билдирилген эмес.
(11) Hemgenix
Компания: UniQure Corporation тарабынан иштелип чыккан.
Базарга чыгуу убактысы: FDA тарабынан 2022-жылдын ноябрында маркетинг үчүн бекитилген.
Көрсөтмөлөр: Гемофилия В менен ооруган чоң кишилерди дарылоо үчүн.
Эскертүү: Hemgenix AAV5 векторунун негизиндеги ген терапиясы.Дары тамырга киргизилүүчү коагуляция фактору IX (FIX) генинин FIX-Padua варианты менен жабдылган.Киргизилгенден кийин ген боордо FIX уюу факторун экспрессиялай алат жана бөлүп чыгара алат, канга киргенден кийин уюу функциясын аткаруу үчүн, дарылоо максатына жетүү үчүн, теориялык жактан алганда, бир кабыл алуу узак убакытка эффективдүү болот.
(12) Адстиладрин
Компания: Ferring Pharmaceuticals тарабынан иштелип чыккан.
Базарга чыгуу убактысы: FDA тарабынан 2022-жылдын декабрь айында маркетинг үчүн бекитилген.
Көрсөтмөлөр: Бацилла Калмет-Гуеринге (БЦЖ) жооп бербеген булчуң-инвазивдик эмес табарсык рагын (NMIBC) дарылоо үчүн.
Эскертүү: Адстиладрин – бул репликацияланбаган аденовирустук векторго негизделген ген терапиясы, ал максаттуу клеткаларда альфа-2b интерферон протеинди ашыкча экспрессиялай алат жана заара чыгаруучу катетер аркылуу табарсыкка киргизилет (үч айда бир жолу), вирустун вектору табарсыктын капталынын клеткаларына эффективдүү түрдө жугушу мүмкүн, андан кийин альфа-2b протеиндерин экспрессияга таасир этет.Бул жаңы ген терапия ыкмасы ошентип, пациенттин табарсык дубалынын клеткаларын интерферонду өндүргөн миниатюралык “фабрикага” айландырат, ошону менен пациенттин рак менен күрөшүү жөндөмдүүлүгүн жогорулатат.
Адстиладриндин коопсуздугу жана натыйжалуулугу көп борборлуу клиникалык изилдөөдө бааланган, анын ичинде BCG-жоопсуз NMIBC коркунучу бар 157 бейтап.Бейтаптар Adstiladrin ар бир үч ай сайын 12 айга чейин, же дарылоо үчүн жол берилгис уулуулугун же жогорку сорттогу NMIBC кайталанган чейин кабыл алды.Жалпысынан, Adstiladrin менен дарыланган катталган бейтаптардын 51 пайызы толук жооп (цистоскопия, биопсия кыртышында жана заара көргөн рактын бардык белгилери жоголуп) жетишти.
3. Майда нуклеин кислотасы препараттары
(1) Vitravene
Компания: Ionis Pharma (мурдагы Isis Pharma) жана Novartis тарабынан биргеликте иштелип чыккан.
Базарга чыгуу убактысы: 1998 жана 1999-жылдары FDA жана EU EMA тарабынан маркетинг үчүн бекитилген.
Көрсөтмөлөр: ВИЧ-позитивдүү пациенттерде цитомегаловирустук ретинитти дарылоо үчүн.
Эскертүү: Vitravene - бул антисенстик олигонуклеотиддик дары, ал дүйнөдө маркетинг үчүн бекитилген биринчи олигонуклеотиддик дары.листингдин баштапкы этабында, анти-CMV дары үчүн рыноктук суроо-талап абдан актуалдуу болгон;кийинчерээк, жогорку активдүү антиретровирустук терапиянын өнүгүшүнө байланыштуу, CMV учурларынын саны кескин кыскарган.Рыноктун жай суроо-талабынан улам, дары 2002-жылы жана 2006-жылы ЕБ өлкөлөрүндө жана АКШда чыгарылган.
(2) Макуген
Компания: Pfizer жана Eyetech тарабынан биргелешип иштелип чыккан.
Базарга чыгуу убактысы: 2004-жылы Кошмо Штаттарда листингге бекитилген.
Көрсөтмөлөр: Неоваскулярдык курактык макулярдык дегенерацияны дарылоо үчүн.
Эскертүү: Макуген - бул пегилирленген модификацияланган олигонуклеотиддик дары, ал тамырдын эндотелийдик өсүү факторун (VEGF165 субтипи) бутага алат жана байланыштыра алат жана башкаруу ыкмасы - интравитреалдык инъекция.
(3) Defitelio
Компания: Jazz Pharmaceuticals тарабынан иштелип чыккан.
Базарга чыгуу убактысы: 2013-жылы Европа Биримдиги тарабынан маркетинг үчүн бекитилген жана 2016-жылдын март айында FDA тарабынан маркетинг үчүн бекитилген.
Көрсөтмөлөр: гемопоэтикалык өзөк клеткасын трансплантациялоодон кийин бөйрөк же өпкө дисфункциясы менен байланышкан боордун вено-окклюзиондук оорусун дарылоо үчүн.
Эскертүү: Дефителио – бул олигонуклеотиддик дары, ал плазминдик касиеттери бар олигонуклеотиддердин аралашмасы.Коммерциялык себептерден улам 2009-жылы базардан чыгарылган.
(4) Kynamro
Компания: Ionis Pharma жана Kastle тарабынан биргелешип иштелип чыккан.
Базарга чыгуу убактысы: 2013-жылы, ал жетим дары катары Кошмо Штаттарда маркетинг үчүн бекитилген.
Көрсөтмөлөр: Гомозиготалуу үй-бүлөлүк гиперхолестеринемияны адъювант дарылоо үчүн.
Эскертүү: Kynamro – антисенстик олигонуклеотиддик дары, ал адамдын апо В-100 мРНКсына багытталган антисенстик олигонуклеотид.Kynamro жумасына бир жолу 200 мг тери астына киргизилет.
(5) Spinraza
Компания: Ionis Pharmaceuticals тарабынан иштелип чыккан.
Базарга чыгуу убактысы: 2016-жылдын декабрь айында маркетинг үчүн FDA тарабынан бекитилген.
Көрсөтмөлөр: Омуртканын булчуңдарынын атрофиясын (SMA) дарылоо үчүн.
Эскертүү: Spinraza (nusinersen) - антисенстик олигонуклеотиддик дары.Спинраза SMN2 экзонунун 7 ажыраган жерине байланышып, SMN2 генинин РНК бөлүнүшүн өзгөртө алат, ошону менен толук иштеген SMN протеининин өндүрүшүн көбөйтөт.2016-жылдын августунда, BIOGEN Spinraza үчүн глобалдык укуктарды алуу үчүн өз тандоосун ишке ашырган.Spinraza өзүнүн биринчи клиникалык сыноосун 2011-жылы гана адамдарда баштаган. Болгону 5 жылдын ичинде, ал FDA тарабынан 2016-жылы маркетинг үчүн жактырылган, бул FDA анын эффективдүүлүгүн толук таануусун чагылдырат.Дары Кытайда маркетинг үчүн 2019-жылдын апрель айында бекитилген. Кытайда Spinraza үчүн бүткүл бекитүү цикли 6 айга жетпеген жана Spinraza Кошмо Штаттарда биринчи жолу бекитилгенден бери 2 жыл 2 ай өттү.Кытайда листингдин ылдамдыгы буга чейин абдан тез.Бул ошондой эле Баңгизаттарды баалоо борбору тарабынан 2018-жылдын 1-ноябрында “Клиникалык практикада шашылыш зарыл болгон чет элдик жаңы дарылардын биринчи партиясын жарыялоо жөнүндө билдирүү” чыгарылып, тездетилген кароо үчүн 40 жаңы чет элдик дары-дармектердин биринчи партиясына киргизилгендиги менен байланыштуу, алардын арасында Spinra орун алган.
(6) Exondys 51
Компания: AVI BioPharma тарабынан иштелип чыккан (кийинчерээк Sarepta Therapeutics деп өзгөртүлгөн).
Базарга чыгуу убактысы: 2016-жылдын сентябрында FDA тарабынан маркетинг үчүн бекитилген.
Көрсөтмөлөр: Дюшен булчуң дистрофиясын (DMD) DMD гениндеги экзон 51 аттап өтүүчү ген мутациясын дарылоо үчүн.
Эскертүү: Exondys 51 – антисенстик олигонуклеотиддик препарат, антисенстик олигонуклеотид DMD генинин пре-мРНКсынын 51 экзонунун абалына туташып, жетилген мРНКнын пайда болушуна алып келет, экзон 51нин бир бөлүгүн алып салуу бөгөттөлүп, мРНКнын кээ бир рамкаларын окууга жардам берет, бул пациенттерге кээ бир рамкаларды кыскартууга жардам берет. кадимки протеинге караганда, ошону менен оорулуунун белгилерин жакшыртат.
(7) Тегседи
Компания: Ionis Pharmaceuticals тарабынан иштелип чыккан.
Базарга чыгуу убактысы: 2018-жылдын июлунда Европа Биримдиги тарабынан маркетинг үчүн бекитилген.
Көрсөтмөлөр: тукум куума транстиретин амилоидозын (hATTR) дарылоо үчүн.
Эскертүү: Tegsedi - бул транстиретин мРНКга багытталган антисенстик олигонуклеотиддик дары.Бул hATTR дарылоо үчүн дүйнөдө бекитилген биринчи дары болуп саналат.Бул тери астына сайынуу жолу менен жүргүзүлөт.Дары транстиретиндин мРНКсын (ATTR) бутага алуу менен ATTR протеининин өндүрүшүн азайтат жана ATTRди дарылоодо жакшы пайда-тобокелдик катышына ээ жана пациенттин нейропатиясы жана жашоо сапаты бир топ жакшырды жана ал TTR мутациясынын түрлөрү менен шайкеш келет, Оорунун стадиясына да, кардиомиопатиянын болушуна да тиешелүү эмес.
(8) Onpatro
Компания: Alnylam Corporation жана Sanofi Corporation тарабынан биргелешип иштелип чыккан.
Базарга чыгуу убактысы: 2018-жылы Кошмо Штаттарда листингге бекитилген.
Көрсөтмөлөр: тукум куума транстиретин амилоидозын (hATTR) дарылоо үчүн.
Эскертүү: Onpattro - бул транстиретин мРНКсына багытталган siRNA препараты, ал боордогу ATTR протеининин өндүрүшүн азайтат жана транстиретиндин mRNAсын (ATTR) бутага алуу менен перифериялык нервдерде амилоиддик депозиттердин топтолушун азайтат, ошону менен оорунун симптомдорун жакшыртат жана басаңдатат.
(9) Givlaari
Компания: Alnylam Corporation тарабынан иштелип чыккан.
Базарга чыгуу убактысы: FDA тарабынан 2019-жылдын ноябрында маркетинг үчүн бекитилген.
Көрсөтмөлөр: Чоңдордогу курч боор порфириясын (АГП) дарылоо үчүн.
Эскертүү: Givlaari - siRNA дары, ал Onpattro кийин маркетинг үчүн бекитилген экинчи siRNA дары болуп саналат.башкаруу ыкмасы тери астына сайма болуп саналат.Дары ALAS1 протеининин мРНКсына багытталган жана Гивлаари менен ай сайын дарылоо боордогу ALAS1 деңгээлин олуттуу жана биротоло төмөндөтөт, ошону менен нейротоксикалык ALA жана PBG деңгээлин нормалдуу диапазонго чейин төмөндөтөт, ошону менен пациенттин оорусунун симптомдорун жеңилдетет.Маалыматтар Givlaari менен дарыланган бейтаптар плацебо тобуна салыштырмалуу талмалардын саны 74% га азайгандыгын көрсөттү.
(10) Vyondys53
КОМПАНИЯ: Sarepta Therapeutics тарабынан иштелип чыккан.
Базарга чыгуу убактысы: FDA тарабынан 2019-жылдын декабрында маркетинг үчүн бекитилген.
Көрсөтмөлөр: Дистрофин генинин экзон 53 сплайсинг мутациясы бар DMD бейтаптарын дарылоо үчүн.
Эскертүү: Vyondys 53 - бул антисенстик олигонуклеотиддик дары, ал дистрофинге чейинки мРНКны бириктирүү процессине багытталган.Exon 53 жарым-жартылай кыскартылган, башкача айтканда, жетилген мРНКда жок жана кесилген, бирок дагы эле функционалдуу дистрофинди өндүрүү үчүн иштелип чыккан, ошону менен пациенттердин көнүгүү жөндөмдүүлүгүн жакшыртат.
(11) Waylivra
Компания: Ionis Pharmaceuticals жана анын туунду компаниясы Akcea Therapeutics тарабынан иштелип чыккан.
Базарга чыгуу убактысы: 2019-жылдын май айында Европалык дарылар агенттиги (EMA) тарабынан маркетинг үчүн бекитилген.
Көрсөтмөлөр: Үй-бүлөлүк хиломикронемия синдрому (FCS) менен ооруган бойго жеткен бейтаптарда диетаны көзөмөлдөөгө кошумча терапия катары.
Эскертүү: Waylivra - бул антисенстик олигонуклеотиддик дары, ал FCS дарылоо үчүн дүйнөдө маркетинг үчүн бекитилген биринчи дары.
(12) Leqvio
Компания: Novartis тарабынан иштелип чыккан.
Базарга чыгуу убактысы: 2020-жылдын декабрында маркетинг үчүн Европа Биримдиги тарабынан бекитилген.
Көрсөтмөлөр: Биринчилик гиперхолестеринемия (гетерозиготалуу үй-бүлөлүк жана үй-бүлөлүк эмес) же аралаш дислипидемиясы бар чоң кишилерди дарылоо үчүн.
Эскертүү: Leqvio PCSK9 mRNA багытталган siRNA дары болуп саналат.Бул холестеролду (LDL-C) төмөндөтүү үчүн дүйнөдөгү биринчи siRNA терапиясы.Бул тери астына сайынуу жолу менен жүргүзүлөт.дары РНК кийлигишүүсү аркылуу PCSK9 белоктун деңгээлин төмөндөтөт, ошону менен LDL-C деңгээлин төмөндөтөт.Клиникалык маалыматтар статиндердин максималдуу жол берилген дозасы менен дарылоодон кийин LDL-C деңгээлин максаттуу деңгээлге түшүрө албаган бейтаптар үчүн Leqvio LDL-Cди болжол менен 50% га азайта аларын көрсөтүп турат.
(13)Окслумо
Компания: Alnylam Pharmaceuticals тарабынан иштелип чыккан.
Базарга чыгуу убактысы: 2020-жылдын ноябрында маркетинг үчүн Европа Биримдиги тарабынан бекитилген.
Көрсөтмөлөр: Биринчи типтеги гипероксалуриянын 1 (PH1) дарылоо үчүн.
Эскертүү: Oxlumo - бул гидрокси-оксидаза 1 (HAO1) mRNAга багытталган siRNA препараты жана башкаруу ыкмасы - тери астына инъекция.Дары Alnylamдын эң акыркы өркүндөтүлгөн стабилдештирүү химиясын, ESC-GalNAc конъюгация технологиясын колдонуу менен иштелип чыккан, ал тери астына siRNAны көбүрөөк туруктуулук жана потенция менен киргизүүгө мүмкүндүк берет.Дары гидроксикислота оксидаза 1 (HAO1) мРНКсын начарлатат же ингибирлейт, боордогу гликолат оксидазасынын деңгээлин төмөндөтөт, андан кийин оксалат өндүрүү үчүн зарыл болгон субстратты керектейт, оксалат өндүрүшүн азайтып, оорулууларда оорунун өнүгүшүн көзөмөлдөө жана оорунун симптомдорун жакшыртуу.
(14) Вилтепсо
Компания: NS Pharma тарабынан иштелип чыккан, Nippon Shinyaku туунду.
Базарга чыгуу убактысы: 2020-жылдын августунда маркетинг үчүн FDA тарабынан бекитилген.
Көрсөтмөлөр: Дюшен булчуң дистрофиясын (DMD) DMD гениндеги экзон 53 өткөрүп жиберүүчү ген мутациясын дарылоо үчүн.
Эскертүү: Вилтепсо – антисенстик олигонуклеотиддик препарат, ал DMD генинин пре-мРНКсынын 53-экзонунун абалына туташып, жетилген мРНК пайда болгондон кийин 53-экзондун бир бөлүгүн алып салууга алып келет, ошону менен мРНКны окуу алкагын жарым-жартылай коррекциялайт. оорулуулардын.
(15) Амондис 45
Компания: Sarepta Therapeutics тарабынан иштелип чыккан.
Базарга чыгуу убактысы: FDA тарабынан 2021-жылдын февралында маркетинг үчүн бекитилген.
Көрсөтмөлөр: Дюшен булчуң дистрофиясын (DMD) DMD гениндеги экзон 45 скип ген мутациясын дарылоо үчүн.
Эскертүү: Amondys 45 - антисенстик олигонуклеотиддик препарат, антисенстик олигонуклеотид DMD генинин пре-мРНКсынын 45-экзонунун абалына байланыша алат, натыйжада жетилген mRNA жаралгандан кийин 45-экзондун бөлүгү бөгөттөлүп калат, ошону менен жарым-жартылай mRNAнын рамкасын окууга жардам берет, кээ бир пациенттерге mRNA-нын кыскача иштешине жардам берет. нормалдуу протеинге караганда er, ошону менен оорулуунун симптомдорун жакшыртат.
(16) Amvuttra (vutrisiran)
Компания: Alnylam Pharmaceuticals тарабынан иштелип чыккан.
Базарга чыгуу убактысы: FDA тарабынан 2022-жылдын июнь айында маркетинг үчүн бекитилген.
Көрсөтмөлөр: Чоңдордогу тукум куума транстиретин амилоидозын полиневропатия (hATTR-PN) менен дарылоо үчүн.
Эскертүү: Amvuttra (Vutrisiran) тери астына сайынуу жолу менен башкарылуучу transthyretin (ATTR) мРНКга багытталган siRNA дары болуп саналат.Vutrisiran Alnylam's Enhanced Stability Chemistry (ESC)-GalNAc конъюгат жеткирүү платформасынын дизайнына негизделген, потенциалы жана метаболизминин туруктуулугу жогорулаган.Терапияны бекитүү анын III фазасынын клиникалык изилдөөсүнүн (HELIOS-A) 9 айлык маалыматтарына негизделген жана жалпы жыйынтыктар терапия hATTR-PN симптомдорун жакшыртып, 50% дан ашыгы бейтаптардын абалын өзгөрткөн же начарлоосун токтоткон.
4. Башка ген терапиясы препараттары
(1) Рексин-Г
Компания: Epeius Biotech тарабынан иштелип чыккан.
Базарга чыгуу убактысы: 2005-жылы Филиппин тамак-аш жана дары-дармек башкармалыгы (BFAD) тарабынан маркетинг үчүн бекитилген.
Көрсөтмөлөр: химиотерапияга туруктуу рактын өнүккөн түрлөрүн дарылоо үчүн.
Эскертүү: Rexin-G – бул ген жүктөлгөн нанобөлүкчөлөрдүн инъекциясы.Ал катуу шишиктерди атайын өлтүрүү үчүн ретровирустук вектор аркылуу максаттуу клеткаларга циклин G1 мутант генин киргизет.башкаруу ыкмасы венага куюу болуп саналат.Метастатикалык рак клеткаларын жигердүү издеген жана жок кылган шишикке багытталган дары катары, башка рак дарыларын, анын ичинде максаттуу биологиялык дарыларды колдонбогон бейтаптарга белгилүү бир айыктыруучу таасир этет.
(2) Neovasculgen
Компания: Адамдын өзөк клеткалары институту тарабынан иштелип чыккан.
Листинг убактысы: 2011-жылдын 7-декабрында Россиянын листингине бекитилген, андан кийин 2013-жылы Украинада ишке киргизилген.
Көрсөтмөлөр: перифериялык тамырлардын артериялык ооруларын, анын ичинде буттун оор ишемияларын дарылоо үчүн.
Эскертүү: Neovasculgen – бул ДНК плазмиддерине негизделген ген терапиясы.Кан тамыр эндотелий өсүү фактору (VEGF) 165 ген плазмиддик омурткада курулуп, бейтаптарга куюлат.
(3) Collategen
Компания: Осака университети жана венчурдук компаниялар тарабынан биргелешип иштелип чыккан.
Базарга чыгуу убактысы: 2019-жылдын августунда Япониянын Саламаттыкты сактоо, эмгек жана жыргалчылык министрлиги тарабынан бекитилген.
Көрсөтмөлөр: Критикалык төмөнкү экстремалдык ишемияларды дарылоо.
Эскертүү: Collategene - бул плазмидага негизделген ген терапиясы, Япониядагы ген терапиясы компаниясы AnGes тарабынан чыгарылган биринчи ата мекендик ген терапиясы.Бул дарынын негизги компоненти адамдын гепатоцитинин өсүү фактору (HGF) ген ырааттуулугун камтыган жылаңач плазмид болуп саналат.Эгерде препарат инъекцияга булчуңдардын ылдыйкы буту, анда айтылган HGF өбөлгө түзүлүшү жаңы кан тамырлардын айланасында жабылган кан тамырлардын.Клиникалык сыноолор анын жараларды жакшыртууга таасирин тастыктады.
Кантип Foregene ген терапиясын өнүктүрүүгө жардам берет?
Биз siRNA дарысын иштеп чыгуунун алгачкы этабында масштабдуу скринингде скрининг убактысын үнөмдөөгө жардам беребиз.
Кененирээк маалымат:
https://www.foreivd.com/cell-direct-rt-qpcr-kit-direct-rt-qpcr-series/
Посттун убактысы: 27-декабрь 2022-жыл